Чехия одобри българския ивермектин за лечение на COVID-19
Решението идва след експертно становище на Държавния институт за контрол на лекарствата
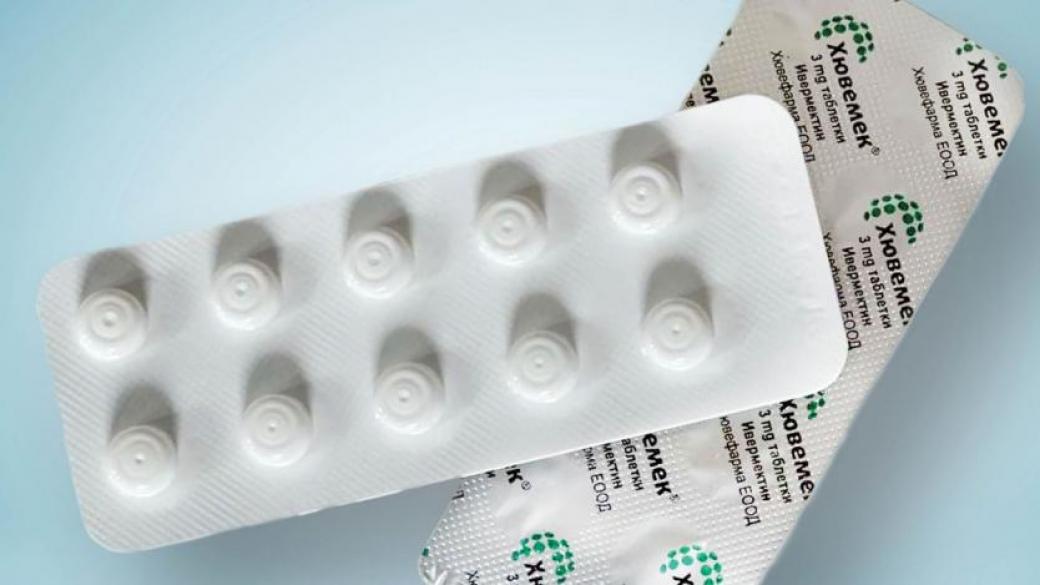
Министерството на здравеопазването на Чехия временно разрешава дистрибуцията, продажбата и използването на българския хуманен лекарствен продукт „Хювемек“, съдържащ активното вещество ивермектин.
Министерството позволява използването на българския ивермектин за лечение на пациенти със заболяването COVID-19 идва след експертно становище на Държавния институт за контрол на лекарствата. Одобрението засега важи до 31 август 2021 г.
Институтът в своето становище е посочил, че активното вещество ивермектин e предназначено първоначално за лечение на паразитни заболявания при човека (филариаза, краста, стронгилоидиаза, онхоцеркоза) и при животните. Лекарствените продукти със съдържание на ивермектин в перорална лечебна форма са регистрирани под различни названия в няколко страни от Европейския съюз и Европейската икономическа общност, но никъде не са регистрирани за лечение на COVID-19.
С оглед на добрия профил по отношение на безопасността и на потенциалните, макар и недоказани клинично, ефекти при лечението на COVID-19, ивермектин представлява възможна алтернатива при подкрепящо лечение на пациенти, хоспитализирани с диагноза коронавирус, се посочва в становището на чешкото здравно министерство, с което се разрешава използването на българския продукт.
Институтът също така е посочил, че препоръките за използване на лекарствените продукти със съдържание на активното вещество ивермектин за лечение на COVID-19 е основано преди всичко върху предположението за възможно понижаване на степента на хоспитализация и подобряване на клиничните признаци при пациенти, по-възрастни от 18 години. Възможното подобрение при протичането на COVID-19 заболяването е отчетено от редица публикувани клинични изследвания, въпреки че някои от тях не достигат до изискваното равнище на медицината, основана на доказателства (Evidence Based Medicine), се посочва още в становището. Но там се напомня, че използването на ивермектин бе въведено масово в Перу, където е било наблюдаван драстичен спад на смъртността от COVID-19.
Освен това, с оглед на благоприятния профил по отношение на безопасността на продукта, и с оглед липсата на други лекарствени алтернативи, Институтът посочва, че е по-подходящо да бъде разрешено използването на нерегистриран лекарствен продукт при контролирани условия и да се избегне по този начин небалансираното използване на ивермектин, придобит на черния пазар или използването на неподходящи ветеринарни продукти, или неподходящи лекарствени форми в (крем, паста).
С оглед на риска от тератогенит лекарственият препарат не трябва да бъде даван на бременни. При лечението с лекарствения продукт „Хювемек“ е необходимо да се проследява функцията на черния дроб преди лечението и след приключване на лечението.
Институтът предлага на Министерството на здравеопазването на Чехия в своето решение да даде възможност за използване на лекарствения продукт "Хювемек", произвеждан от фармацевтичната компания "Хювефарма", за лечение на заболяването COVID-19 при хоспитализирани възрастни пациенти при условие, че лечението е започнато възможно най-рано след приемане в болница. Причината за ограничението за използване на лекарствения продукт "Хювемек" само при хоспитализирани пациенти е необходимостта от проследяване на безопасността на лечението.